Le 29 décembre dernier, une loi a été signée autorisant la Food and Drug Administration (FDA) – l’agence fédérale américaine des produits alimentaires et médicamenteux – à avoir recours à des méthodes alternatives en lieu de tests sur animaux avant d’approuver le passage d’un traitement en phase clinique chez l’humain. Le Gircor fait le point sur l’envers de cette annonce et ses conséquences avec Philippe Detilleux, directeur mondial de la toxicologie chez Sanofi et spécialiste du sujet.
Quels sont les tests concernés par l’annonce de la FDA et en quoi consistent-ils ?

Philippe Detilleux : Il est question des tests portant sur l’innocuité et l’efficacité d’un médicament qui sont obligatoires avant de les soumettre à des essais cliniques chez l’humain. La toxicologie vise à mesurer les effets de molécules biologiquement actives et à réduire le risque chez les patients en identifiant la nocivité pour l’organisme.
En pratique, nous connaissons toujours la cible thérapeutique d’un traitement en cours de développement, c’est-à-dire là où la molécule est censée agir. Or en toxicologie, nous ne nous focalisons pas uniquement sur cet effet, mais aussi sur tout ce qui pourrait se passer par ailleurs. Autrement dit : si une molécule va agir sur la cible visée, elle peut aussi agir sur d’autres parties du corps. Par exemple, l’aspirine bloque les prostaglandines, des cytokines responsables de l’inflammation. Or, celles-ci sont également impliquées dans la protection de la muqueuse gastrique et modulent la vascularisation du rein. Si bien qu’à une certaine dose, l’aspirine peut générer des ulcères gastriques et d’autres effets néfastes au niveau rénal. Il s’agit d’un effet spécifique qui n’était pas celui escompté.
Un autre type d’effet recherché est lié à la structure de la molécule développée. Lorsque celle-ci est synthétique, nous voulons identifier toutes les informations liées à sa toxicité chimique. Elle peut présenter des impuretés, ou alors son interaction avec notre métabolisme peut créer des effets nocifs non anticipés. Ceci n’est pas le cas pour les molécules d’origine biologiques comme par exemple, des traitements ayant recours à des anticorps, pour lesquelles on peut se permettre de réaliser moins d’études sur leur toxicité. Le type de molécule détermine le choix du modèle – ou plutôt la combinaison de modèles – la plus adaptée à l’étude du profil toxicologique.
Ces tests sont réalisés de façon systématique. Sont-ils pour autant réalisés sur des animaux ?
P.D. : Nombre d’efforts ont été mis en œuvre pour réduire, remplacer et raffiner les tests sur les animaux en amont des essais cliniques. La recherche de risques mutagènes liés aux impuretés, c’est-à-dire de résidus associés à la synthèse chimique d’un médicament, est par exemple menée à l’aide de modèles informatiques. Aujourd’hui, si ces tests ne détectent aucune alerte, alors nous avons un niveau de confiance suffisant dans ces outils pour considérer qu’il n’est pas nécessaire de réaliser d’expériences sur les animaux.
De même, des essais in vitro sont mis en place lorsque nous sommes confrontés à des toxicités connues ou traitons des cibles déjà étudiées. Plus généralement, lorsque nous savons déjà où et quoi regarder, il est plus facile de remplacer l’animal.
Qu’est-ce que l’annonce de la FDA va changer à ce contexte ?
P.D. : Cette annonce ne signifie pas que les autorités américaines autorisent la mise sur le marché de médicaments sans recourir à l’expérimentation animale. La nouveauté est d’avoir inclus les méthodes alternatives telles que les organes sur puce, les approches de prédiction par ordinateurs, etc. dans les textes réglementaires, en plus du recours aux animaux. La FDA a donc clarifié sa position sur le sujet. Or, pour qu’une méthode alternative prenne le pas sur les essais sur animaux, il faut prouver qu’elle est au moins aussi prédictive. Ou alors, démontrer que le modèle animal n’est pas adapté à l’étude toxicologique.
Désormais, la question est de savoir la vitesse à laquelle cette prise de position va vraiment faire évoluer la situation. En tant qu’industrie, nous sommes obligés d’en revenir aux faits et à la science. Nous adoptons déjà une approche raisonnée et lorsque nous sommes en capacité de démontrer que les tests sur animaux ne sont pas pertinents, nous le défendons auprès des autorités. Fondamentalement, la FDA ne fait que mettre sur papier quelque chose qu’elle acceptait déjà en pratique et au cas par cas depuis longtemps.
Il y a donc déjà eu des cas où les autorités ont permis des essais cliniques sans étude préalable menée sur l’animal ?
P.D. : C’est très rare, mais c’est possible. Cela a été le cas notamment pour un traitement anti-cancéreux de Sanofi à base d’anticorps disponible depuis peu sur le marché français. Lors de son développement, le traitement ne fonctionnait que chez l’humain. Nous avons approché les autorités de santé, aux États-Unis et en France, en expliquant qu’aucun modèle animal ne permettrait d’étudier l’effet fonctionnel escompté de l’anticorps. Il y a eu un important argumentaire et notre demande a été acceptée. Nous avons réalisé des essais chez l’homme uniquement après avoir mené des tests in vitro sur des cellules humaines. Les premières doses autorisées chez l’homme ont par contre été très faibles et la première étude clinique plus longue afin de réduire le risque.
Ce qu’il faut retenir, c’est qu’il est possible dans des cas exceptionnels de se passer d’études animales, mais ce ne sera pas systématique. Cela est intimement lié à la notion de bénéfice/risque. À chaque fois, l’enjeu est de prouver que nous ne prendrons pas de risques qui auraient pu être identifiés avant la mise en place des essais sur l’humain. Les méthodes alternatives sont plus facilement acceptées dans le cadre de traitements contre des maladies rares, car il n’y a pas d’autres issues pour le patient.
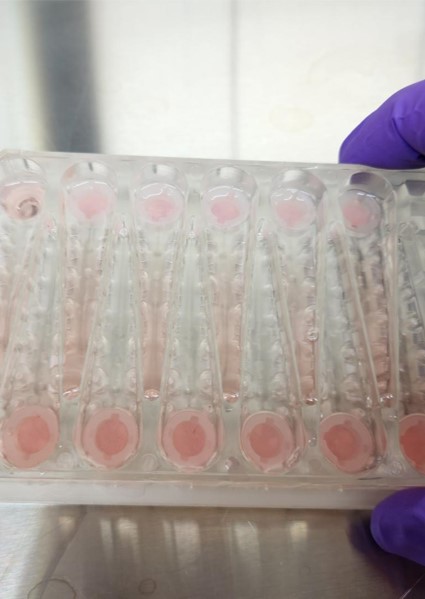
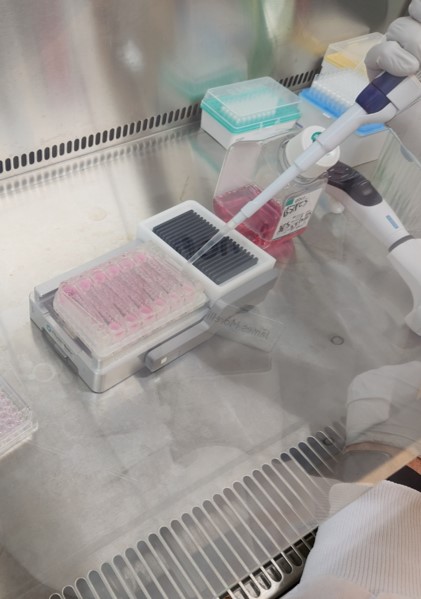

Plaques microfluididiques pour la culture d’organoïdes de foie ©Sanofi
Les modèles alternatifs sont-ils pour autant suffisamment matures technologiquement pour remplacer l’animal ?
P.D. : Beaucoup de modèles s’améliorent. Le foie est, par exemple, une cible classique en toxicologie. Auparavant, nous réalisions des cultures sur plaque en 2D qui ne contenaient que des hépatocytes et ne permettait de détecter qu’un petit nombre de molécules toxiques. Désormais, ces tests sont réalisés sur des sphéroïdes 3D qui contiennent d’autres cellules du foie et permettent de détecter plus de molécules nocives. Cependant, chaque modèle répond à des questions spécifiques, mais pas à toutes.
Or, lorsqu’il est question d’évaluer les effets d’une nouvelle molécule sur une cible qui n’a jamais été testée chez l’homme, il faut identifier tous les risques potentiels. Le seul sujet qui nous permet d’envisager toutes les possibilités, c’est l’humain. Et juste avant, c’est l’animal vivant avec les interdépendances entre ses organes, son comportement et ses effets physiologiques. Encore avant, ce sont des simulations informatiques et des modèles in vitro qui nous permettent de mener les études sur les animaux dans des conditions optimales.
Qu’en est-il de la situation réglementaire en Europe ?
P.D. : En général, l’Europe est plus sensible à la réduction de l’utilisation des animaux. Il y a des efforts au niveau de l’industrie et des autorités avec la mise en place de stratégies 3R. Par exemple, il existe une évolution des recommandations sur les études de carcinogénicité qui visent à identifier le risque que les candidats médicaments engendrent des tumeurs chez les animaux en les traitant pendant deux ans. L’Europe a été motrice et la FDA a suivi, de sorte qu’aujourd’hui, nous pouvons déposer des argumentaires sur l’utilité de la méthode et ce qu’elle apporte au cas par cas au point de pouvoir nous en passer si besoin.
Il existe également de nombreuses initiatives en partenariat avec l’Agence européenne des médicaments qui évaluent et promeuvent le déploiement de méthodes alternatives. Dans ce cadre, nous travaillons, par exemple, à l’adoption de groupes de contrôle virtuels en remplacement d’animaux dans les études. Par ailleurs, les partenariats public/privé européens en matière de santé innovante (IMI et désormais Innovative Health Initiative – IHI) sont des programmes auxquels nous avons collaboré et continuons de le faire dans le but de proposer de nouveaux médicaments tout en réduisant et remplaçant les animaux utilisés au cours de leur développement.
En 2021, 28% des utilisations d’animaux à des fins scientifiques en France l’étaient pour les études toxicologiques et réglementaires (contre 31% en 2020 et 29% en 2019).
Qu’est-ce qui, selon vous, pourrait davantage faire bouger les lignes afin de réduire ou remplacer le recours à l’animal en lien avec les essais cliniques ?
P.D. : Je pense que l’industrie peut encore faire d’importants efforts sur le partage d’informations. Bien que nos molécules soient différentes, nous travaillons souvent sur les mêmes cibles et réalisons donc tous des études qui démontreront quelque chose qu’un concurrent a peut-être déjà vu auparavant. Mon avis personnel est que nous ne devrions pas utiliser la sécurité d’un médicament comme un avantage compétitif.
Dans le cadre des projets IMI-IHI, nous avons justement démontré qu’on gagnait plus à partager des données qu’à les garder pour soi. L’Europe s’engage justement dans cette direction avec une volonté de publier les résultats de façon ouverte. Elle vient d’ailleurs de mettre en place un système unique et centralisé pour les essais cliniques. Lié à cela, figure une clause de transparence stipulant qu’elle va mettre à disposition l’ensemble des documents en lien avec un essai clinique tout en protégeant les données personnelles. Actuellement, des dérogations et/ou clauses de confidentialité sont accordées aux industriels qui mènent les essais, mais je m’attends à ce que les autorités de santé demandent davantage de justifications, car ces informations finiront par être publiques une fois le produit sur le marché. Cette approche plus ouverte pourrait être bénéfique au développement de thérapies et à la réduction des tests sur animaux qui leur sont associés.
Philippe Detilleux est un employé de Sanofi et, à ce titre, peut être détenteur d’actions dans la compagnie.
Propos recueillis par Anaïs Culot pour le Gircor

