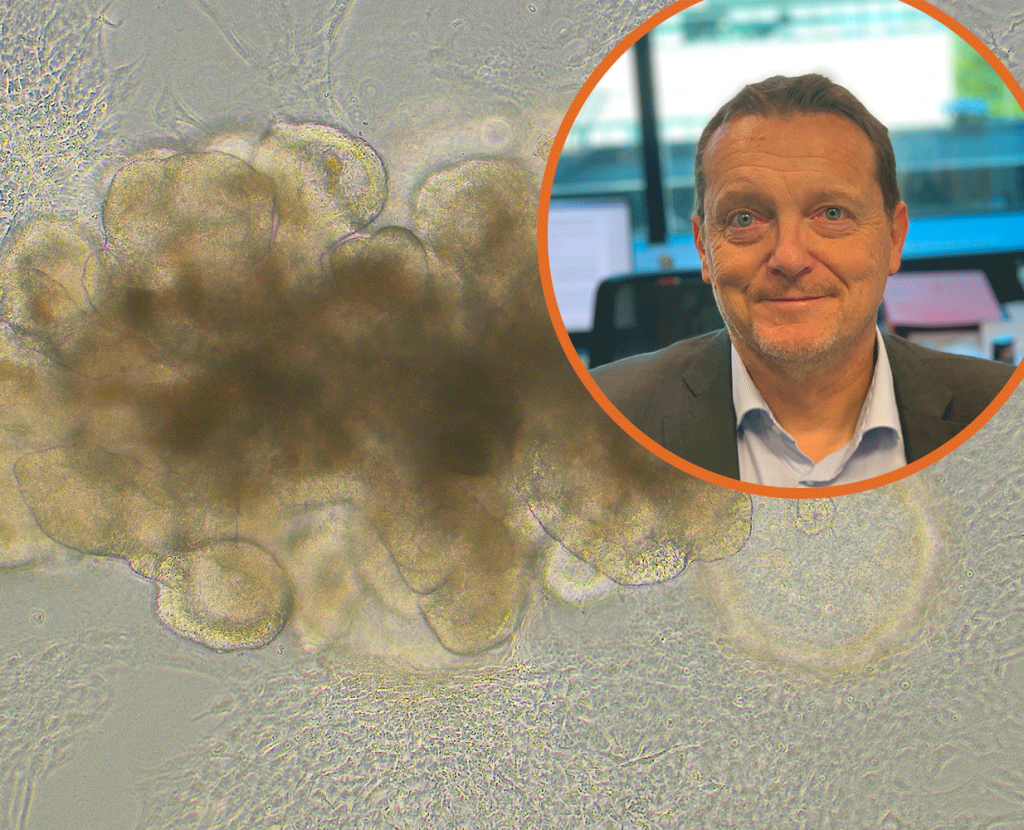
Depuis plus de 30 ans, les organoïdes – des reproductions in vitro et réduites de la structure et l’anatomie d’organes – se développent comme support expérimental au sein des laboratoires. Mais sont-ils à même de remplacer l’utilisation d’animaux à des fins scientifiques comme cela est souvent mentionné dans le débat sur le sujet ? Afin de mieux appréhender les avantages et inconvénients des modèles animaux et organoïdes, le Gircor s’est entretenu avec Gérard Gradwohl, Directeur de recherche à l’Inserm et spécialiste en biologie du développement. Avec son équipe à l’Institut de génétique et de biologie moléculaire et cellulaire (IGBMC – CNRS/Inserm/Université de Strasbourg), il utilise ces deux modèles afin de mieux comprendre le fonctionnement de nos cellules endocrines.
Quel est l’objectif de vos recherches et quels modèles expérimentaux utilisez-vous à cet effet ?
Gérard Gradwohl : Nous nous intéressons aux mécanismes de différenciation des cellules souches en cellules hautement spécialisées, c’est-à-dire la façon dont elles acquièrent des propriétés bien définies. Notre objectif est de comprendre plus particulièrement comment sont générées les cellules endocrines au niveau du pancréas et de l’intestin telles que les cellules bêta qui sécrètent de l’insuline en réponse à notre prise de glucose. L’idée est d’identifier de nouveaux gènes impliqués dans le développement et la spécialisation des cellules jusqu’à ce qu’elles soient matures et fonctionnelles dans notre corps.
Nos travaux de recherche fondamentale contribuent, par exemple, aux connaissances nécessaires au développement de nouvelles thérapies pour le diabète de type 1 basées sur la culture in vitro de cellules productrices d’insuline à partir de cellules souches pluripotentes. Pour notre recherche, nous utilisons à la fois des modèles expérimentaux animaux avec la souris et des systèmes de culture d’organoïdes de pancréas et d’intestin. Ces derniers sont soit dérivés de la souris, soit générés par différentiation de cellules souches pluripotentes induites humaines.
Comment s’articule l’utilisation de ces deux modèles dans vos recherches ?
GG : Nous combinons les deux. Par exemple, nous générons des mutations chez la souris pour étudier leurs conséquences sur la physiologie intestinale. Puis nous dérivons des modèles organoïdes d’intestins à partir de ces animaux sur lesquels il est plus facile de faire de l’imagerie en temps réel et d’étudier les processus de différenciation.
À partir de cellules souches pluripotentes induites humaines, nous fabriquons également des cellules bêta in vitro. Ces cellules produites dans la boîte de Pétri sont immatures. Et pour des raisons que nous ne connaissons pas encore, la transplantation chez l’animal est nécessaire pour qu’elles deviennent fonctionnelles et que la sécrétion d’insuline en réponse au glucose soit efficace. Chaque modèle a don ses avantages et sert à des manipulations qui ne peuvent pas être mises en place chez l’autre ce qui en fait des modèles parfaitement complémentaires.
Pour quels types d’études le modèle animal est-il le plus adapté ?
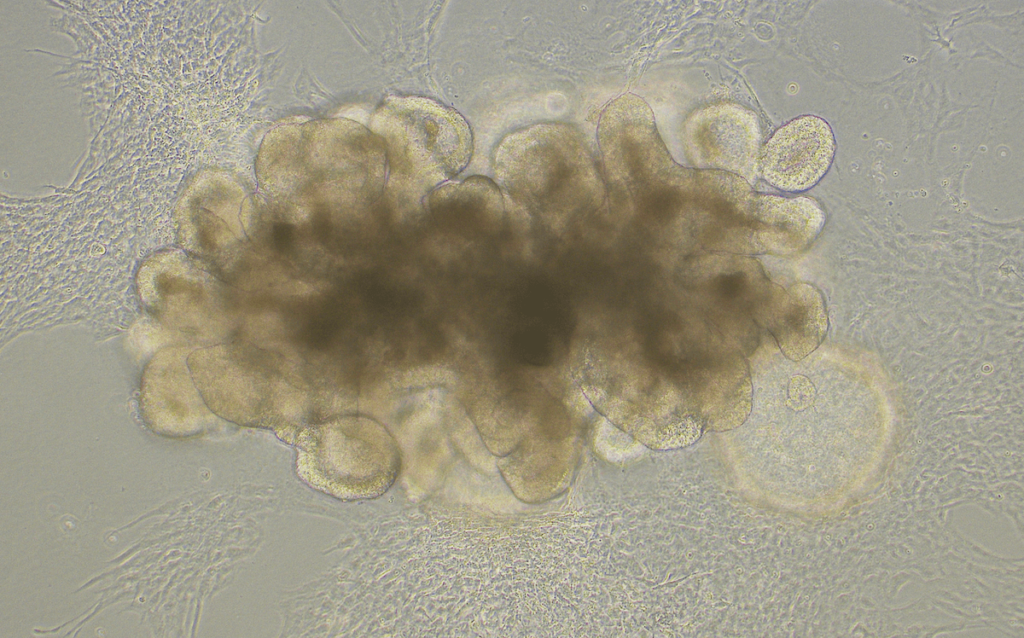
GG : Il y a cette idée reçue que les animaux ne servent qu’à tester des médicaments en laboratoire. Or, bien avant de tester des thérapies, il faut comprendre le développement et la physiologie des êtres vivants, c’est-à-dire la mise en place, les fonctions et les propriétés de leurs organes et de leurs tissus. Les recherches fondamentales sur les animaux permettent ainsi de générer des hypothèses quant aux voies de signalisation ou des molécules à cibler lors de futures thérapies. C’est également grâce aux connaissances acquises chez l’animal, en particulier sur leur développement embryonnaire et de la différentiation des tissus, que la technologie des organoïdes s’est développée.
Que permet de faire le modèle animal contrairement au modèle organoïde ?
GG : Il est possible de générer des organoïdes de nombreux organes, mais ces modèles sont très simplifiés. Par exemple, un organoïde d’intestin est surtout composé de cellules épithéliales alors que cet organe contient également des couches musculaires et un système nerveux. De plus, il communique avec d’autres organes comme le pancréas et l’estomac, ou encore le cerveau.
Donc pour étudier, par exemple, le métabolisme du glucose, son absorption intestinale puis son assimilation par les tissus au sein d’un organisme vivant cela nécessite d’observer un système intégré dans lequel les organes communiquent entre eux. En ce sens, l’animal est donc un modèle plus adapté à des études de physiologie. Un autre avantage, est de pouvoir étudier des aspects sexe-dépendants chez l’animal qui sont plus difficiles à mettre en évidence sur des organoïdes.
Inversement, quels avantages présentent les organoïdes ?
GG : Le fait qu’ils ne constituent pas un système intégré peut parfois être un avantage. En proposant des modèles simplifiés, ils permettent de disséquer des mécanismes de différenciation cellulaire tout en s’affranchissant d’interférences avec d’autres organes. Autre intérêt : un même organoïde d’intestin peut être repiqué de nombreuses fois jusqu’à six mois ou un an. Ils sont ainsi très intéressants dans le cadre d’expériences longitudinales qui suivent l’évolution de populations de cellules sur de longues durées.
Par ailleurs, des organoïdes dérivés de cellules pluripotentes souches humaines sont plus proches d’un tissu fœtal qu’adulte. C’est une caractéristique très intéressante pour mimer et étudier le développement d’organes humains, ce qui n’était pas possible avant.
Les organoïdes humains et ceux issus de souris ont-ils le même impact sur la recherche ?
GG : Il faut bien dissocier les deux. Les organoïdes dérivés de la souris permettent de réduire le nombre d’animaux en étudiant certains processus biologiques en dehors de l’animal vivant. Ils se placent donc en prolongement de l’animal. Au cours des trois dernières années, leur usage nous a permis de réduire de 25 % le nombre de souris utilisées.
Les organoïdes humains nous offrent, quant à eux, un nouveau modèle d’étude permettant d’établir entre autre des modèles de pathologies humaines monogéniques. En inactivant des gènes dans les cellules souches pluripotentes induites humaines, il est possible de générer des « organes » mutants et d’étudier les conséquences sur leur fonctionnement. Il est aussi possible, dans certains cas, de fabriquer des organoïdes à partir de biopsies et donc de tumeurs chez des patients à des fins de médecine personnalisée. Ils servent ainsi à observer in vitro la réaction d’une tumeur à des traitements.
Le modèle organoïde est une technologie encore jeune et en cours de perfectionnement. Quelles sont ses limites actuelles en comparaison au modèle animal ?
GG : La culture de systèmes organoïdes est longue, sophistiquée et couteuse. La différenciation in vitro afin de réaliser un intestin prend entre un et deux mois. De plus, les facteurs de croissance utilisés pour générer un organoïde et le maintenir en vie sont très chers. Il y a également une forte demande pour le matrigel, un produit utilisé dans la plupart des systèmes de culture d’organoïdes, qui cause parfois des pénuries mondiales et peut mettre nos expériences à l’arrêt.
Un autre désavantage des organoïdes est, à mon avis, la reproductibilité des résultats entre laboratoires. Les niveaux d’expertise et les protocoles pour produire et maintenir les organoïdes en vie nécessitent d’être standardisés. Toutefois, tous les organoïdes ne répondent pas aux mêmes règles. Par exemple, les expériences se reproduisent plus facilement dans l’intestin que dans le pancréas, car les protocoles sont mieux maîtrisés. Demeurent néanmoins d’importantes variations expérimentales qui sont bien moins prononcées chez la souris.
Quelles promesses offre alors la combinaison des deux modèles : animal et organoïde ?
GG : La greffe chez l’animal reste un processus nécessaire aujourd’hui pour étudier certains organoïdes et leurs fonctionnalités, car on ne sait pas encore produire in vitro des organes identiques aux organes adultes. Néanmoins, ces derniers sont de plus en plus sophistiqués. À titre d’exemple, il est possible de produire des organoïdes intestinaux innervés. Se développent aussi des méthodes d’organe sur puce qui visent à reproduire les interconnexions physiologiques entre les organes et à mesurer leurs échanges en connectant différents organoïdes. Cependant, la biologie d’un être vivant ne se résume pas simplement à la somme de versions simplifiées de ses organes. C’est pourquoi, les expérimentations ont encore besoin de combiner ces deux modèles. Si les organoïdes permettent donc de réduire le nombre d’animaux, ils ne sont pas assez complexes aujourd’hui pour les remplacer.
Propos recueillis par Anaïs Culot pour le Gircor
Crédits photo : Gérard Gradwohl, IGBMC, Illkirch, France